Lithium Batterien hunn d'Virdeeler vu Portabilitéit a séier Laden, also firwat si Bläi-Sauer Batterien an aner sekundär Batterien nach ëmmer um Maart zirkuléieren?
Zousätzlech zu de Probleemer vu Käschten a verschiddene Applikatiounsfelder ass en anere Grond Sécherheet.
Lithium ass dat aktivste Metal op der Welt.Well seng chemesch Charakteristiken ze aktiv sinn, wann Lithium-Metall un der Loft ausgesat ass, wäert et eng hefteg Oxidatiounsreaktioun mat Sauerstoff hunn, sou datt et ufälleg ass fir Explosioun, Verbrennung an aner Phänomener.Zousätzlech wäert Redoxreaktioun och an der Lithium Batterie optrieden wärend der Opluedung an Entladung.Explosioun a spontan Verbrennung sinn haaptsächlech duerch d'Akkumulation, Diffusioun a Verëffentlechung vun Lithium Batterie no Heizung verursaacht.Kuerz gesot, Lithium-Batterien wäerte vill Wärme während dem Oplued- an Entladungsprozess generéieren, wat zu der Erhéijung vun der interner Temperatur vun der Batterie an der ongläicher Temperatur tëscht eenzelne Batterien féiert, sou datt déi onbestänneg Leeschtung vun der Batterie verursaacht.
Onsécher Verhalen vun der thermescher oflafend Lithium-Ion Batterie (inklusiv Batterie Iwwerbelaaschtung an Iwwerentladung, séier Ladung an Entladung, Kuerzschluss, mechanesch Mëssbrauchsbedéngungen, Héichtemperatur thermesch Schock, etc.) wäerte méiglecherweis geféierlech Säitreaktiounen an der Batterie ausléisen an Hëtzt generéieren, direkt beschiedegt de passive Film op der negativ Elektroden a positiv Elektroden Uewerfläch.
Et gi vill Grënn fir thermesch Runaway Accidenter vu Lithium Ion Batterien ausléisen.Geméiss de Charakteristiken vum Ausléiser kann et a mechanesch Mëssbrauch Ausléisung, elektresch Mëssbrauch Ausléisung an thermesch Mëssbrauch Ausléisung opgedeelt ginn.Mechanesch Mëssbrauch: bezitt sech op Akupunktur, Extrusioun a schwéieren Objeten Impakt duerch Gefier Kollisioun verursaacht;Elektresch Mëssbrauch: allgemeng verursaacht duerch falsch Spannungsmanagement oder elektresch Komponentfehler, inklusiv Kuerzschluss, Iwwerlaaschtung an Iwwerentladung;Hëtztmëssbrauch: verursaacht duerch Iwwerhëtzung verursaacht duerch falsch Temperaturmanagement.
Dës dräi Ausléisermethoden si matenee verbonnen.Mechanesch Mëssbrauch wäert allgemeng Verformung oder Broch vun der Batterie Blend verursaachen, wat zu engem direkte Kontakt tëscht de positiven an negativen Pole vun der Batterie a Kuerzschluss resultéiert, wat zu elektresche Mëssbrauch resultéiert;Wéi och ëmmer, ënner der Bedingung vum Stroummëssbrauch, erhéicht d'Hëtztgeneratioun wéi Joule Hëtzt, wat d'Batterietemperatur eropgeet, wat sech zu Hëtztmëssbrauch entwéckelt, weider d'Kettentyp Wärmegeneratiounssäitreaktioun bannent der Batterie ausléisen, a schliisslech zu der Optriede féiert. vun Batterie Hëtzt Lafen.
D'Batterie thermesch Flucht gëtt verursaacht duerch d'Tatsaach datt d'Hëtztgeneratiounsquote vun der Batterie vill méi héich ass wéi d'Hëtztvergëftungsquote, an d'Hëtzt ass a grousse Betrag accumuléiert awer net an der Zäit opgeléist.Am Wesentlechen ass "thermesch Flucht" e positiven Energie-Feedback-Zyklusprozess: d'Erhéijung vun der Temperatur wäert de System waarm ginn, an d'Temperatur wäert eropgoen nodeems de System waarm gëtt, wat am Tour de System méi waarm gëtt.
De Prozess vun der thermescher Auslafe: wann d'Batterie intern Temperatur eropgeet, de SEI Film op der Uewerfläch vum SEI Film zerstéiert ënner héijer Temperatur, de Lithium-Ion, deen am Grafit agebonnen ass, reagéiert mam Elektrolyt an dem Bindemëttel, dréckt d'Batterietemperatur weider erop. bis 150 ℃, an eng nei gewalteg exotherm Reaktioun wäert bei dëser Temperatur geschéien.Wann d'Batterietemperatur iwwer 200 ℃ erreecht, zerfällt d'Kathodematerial, a léisst eng grouss Quantitéit un Hëtzt a Gas eraus, an d'Batterie fänkt un ze bulgen a kontinuéierlech erhëtzt.D'Lithium embedded Anode huet ugefaang mam Elektrolyt bei 250-350 ℃ ze reagéieren.Dat gelueden Kathodematerial fänkt eng gewalteg Zersetzungsreaktioun un, an den Elektrolyt mécht eng gewalteg Oxidatiounsreaktioun, befreit eng grouss Quantitéit un Hëtzt, generéiert héich Temperaturen an eng grouss Quantitéit vu Gas, verursaacht Verbrennung an Explosioun vun der Batterie.
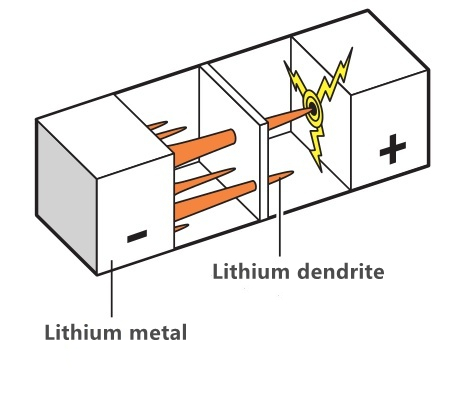
De Problem vum Lithium-Dendrit-Nidderschlag während der Iwwerlaaschtung: Nodeems d'Lithium-Kobalat-Batterie voll gelueden ass, bleift eng grouss Quantitéit vu Lithium-Ionen an der positiver Elektrode.Dat heescht, d'Kathode kann net méi Lithium-Ionen un d'Kathode befestegt halen, awer am iwwerlaaschte Staat schwammen déi iwwerschësseg Lithium-Ionen op der Kathode nach ëmmer an d'Kathode.Well se net voll enthale kënnen, gëtt Metalllithium op der Kathode bilden.Well dëst Metalllithium en dendritesche Kristall ass, gëtt et Dendrit genannt.Wann den Dendrit ze laang ass, ass et einfach d'Diaphragma duerchzebriechen, wat intern Kuerzschluss verursaacht.Well den Haaptkomponent vum Elektrolyt Karbonat ass, sinn säin Zündpunkt a Kachpunkt niddereg, sou datt et bei héijer Temperatur verbrennt oder souguer explodéiert.
Wann et eng Polymer Lithium Batterie ass, ass den Elektrolyt kolloidal, wat ufälleg ass fir méi hefteg Verbrennung.Fir dëse Problem ze léisen, probéieren d'Wëssenschaftler méi sécher Kathodematerial ze ersetzen.D'Material vun der Lithium Manganat Batterie huet gewësse Virdeeler.Et kann dofir suergen, datt de Lithium-Ion vun der positiver Elektrode komplett an d'Kuelestoffloch vun der negativer Elektrode ënner dem Vollladungszoustand agebaut ka ginn, anstatt gewësse Reschter an der positiver Elektrode wéi Lithiumkobalat ze hunn, wat zu engem gewësse Mooss d'Generatioun vun dendrites.Déi stabil Struktur vu Lithiummanganat mécht seng Oxidatiounsleeschtung vill méi niddereg wéi déi vu Lithiumkobalat.Och wann et eng extern Kuerzschluss ass (anstatt eng intern Kuerzschluss), kann et am Fong d'Verbrennung an d'Explosioun duerch Lithium-Metall-Nidderschlag vermeiden.Lithium Eisenphosphat huet méi héich thermesch Stabilitéit a manner Oxidatiounskapazitéit vum Elektrolyt, sou datt et héich Sécherheet huet.
D'alternd Attenuatioun vun der Lithium-Ionbatterie gëtt duerch Kapazitéitattenuatioun an intern Resistenzerhéijung manifestéiert, a säin internen Alterungsdämpfungsmechanismus enthält Verloscht vu positiven an negativen aktive Materialien a Verloscht vu verfügbare Lithiumionen.Wann d'Kathodematerial al a verfall ass, an d'Kapazitéit vun der Kathode net genuch ass, ass de Risiko vun der Lithium-Evolutioun vun der Kathode méi wahrscheinlech optrieden.Ënnert der Bedingung vun der Iwwerflëssegkeet wäert d'Potenzial vu Kathode op Lithium op iwwer 3V eropgoen, wat méi héich ass wéi d'Opléisungspotenzial vu Kupfer, wat d'Opléisung vum Kupfersammler verursaacht.Opgeléist Kupferione fällt op der Kathodeoberfläche aus a bilden Kupferdendriten.Kupfer Dendriten passéieren duerch d'Membran, verursaacht intern Kuerzschluss, wat d'Sécherheetsleistung vun der Batterie eescht beaflosst.
Zousätzlech wäert d'Iwwerladungsresistenz vun alternd Batterien zu engem gewësse Mooss erofgoen, haaptsächlech wéinst der Erhéijung vun der interner Resistenz an der Ofsenkung vu positiven an negativen aktive Substanzen, wat zu der Erhéijung vun der Joule Hëtzt während dem Iwwerlaaschtungsprozess vun de Batterien resultéiert.Ënner manner Iwwerbelaaschtung kënne Säitreaktiounen ausgeléist ginn, wat d'thermesch Oflaf vun de Batterien verursaacht.Wat d'thermesch Stabilitéit ugeet, wäert d'Lithium-Evolutioun vun der Kathode zu engem schaarfen Réckgang vun der thermescher Stabilitéit vun der Batterie féieren.
An engem Wuert, d'Sécherheetsleeschtung vun der aler Batterie gëtt staark reduzéiert, wat d'Sécherheet vun der Batterie eescht a Gefor bréngt.Déi heefegst Léisung ass d'Batterie-Energielagerungssystem mat engem Batteriemanagementsystem (BMS) ze equipéieren.Zum Beispill kënnen d'8000 18650 Batterien, déi am Tesla Model S benotzt ginn, Echtzäit Iwwerwaachung vu verschiddene physikalesche Parameter vun der Batterie realiséieren, de Batterieverbrauchsstatus evaluéieren an Online Diagnostik a fréi Warnung duerch säi Batteriemanagementsystem maachen.Zur selwechter Zäit kann et och Entladung a Pre-Ladekontroll, Batteriebalancemanagement an thermesch Gestioun maachen.
Post Zäit: Dez-02-2022